|
nadtlenek wodoru
Nadtlenek wodoru (ditlenek wodoru, dioksydan)
Nadtlenek wodoru jest związkiem nieorganicznym należącym do grupy nadtlenków.
Wzór chemiczny
Sumaryczny:
H2O2
Strukturalny
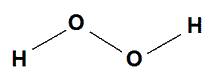
Z budowy cząsteczki nadtlenku wodoru, wynika, że wiązanie pomiędzy atomami tlenu (tzw.
mostek tlenowy) za pomocą jednej wartościowości jest nietrwałe.
Właściwości fizyczne
|
|
|
|
Barwa
|
bezbarwna
|
|
Zapach
|
bezwonny
|
|
|
1,5 g/cm3
|
|
|
miesza się z wodą w każdym stosunku |
Właściwości chemiczne
Nadtlenek wodoru jest związkiem nietrwałym i nawet w temperaturze pokojowej ulega samorzutnemu rozkładowi z wydzieleniem tlenu.
2H2O2 -> 2H2O + O2
Przejściowo powstaje tlen atomowy (tlen in statu nascendi).
Wykazuje słabe własności kwasowe. W roztworach wodnych ulega on dysocjacji według równania:
H2O2 + H2O -> H3O+ (kation hydroniowy) + H-O-O- (anion wodoronadtlenowy)
Nadtlenek wodoru jest silnym utleniaczem. W czasie reakcji utleniania może mieć miejsce albo przeniesienie
tlenu do współregenta (n.p. SO2 -> SO3) lub też przekazanie elektronów
(n.p. Fe2+ -> Fe3+).
W stosunku do silnych środków utleniających takich, jak n.p.: nadmanganian potasu, nadtlenek wodoru może działać jako reduktor. Powstaje przy tym tlen.
W reakcji podstawienia nadtlenek wodoru może przekazywać grupę nadtlenową związkom organicznym i nieorganicznym.
Zagrożenia
Nadtlenek wodoru i jego pary przyczyniają się do powstania na skórze (w przypadku roztworów o stężeniach powyżej 10%)
oraz na śluzówkach (w przypadku roztworów o stężeniach powyżej 5%) białego zabarwienia wierzchniej warstwy. W przypadku krótkotrwałego
zetknięcia się wyżej wymienionych części ze stężonym roztworem nadtlenku wodoru, w miejscu kontaktu powstają martwe, białe, ostro rozgraniczone i w różnym stopniu
swędzące plamy, mylone często z oparzeniami. W rzeczywistości jest to pęcherzenie tkanki wywołane dyfuzją roztworu nadtlenku wodoru do
skóry z jednoczesnym przekazywaniem pęcherzyków tlenu do tkanki skórnej.
Mieszaniny stężonych roztworów nadtlenku wodoru z ciekłymi lub stałymi, rozpuszczalnymi substancjami organicznymi w pewnych określonych stosunkach ilościowych
wykazują właściwości wybuchowe i mogą wybuchnąć pod wpływem niewielkiego pobudzenia mechanicznego lub
termicznego. Jeśli zawartość nadtlenku wodoru w mieszaninie wynosi poniżej 30% nie należy się na ogół obawiać
detonacji. Także w takich przypadkach ważne znaczenie dla zapobiegania powstawaniu mieszanin wybuchowych ma kolejność łączenia składników. Wodne
roztwory o stężeniu do ok. 90% H2O2 nie są wybuchowe. Roztwory o stężeniach od 90 do 100% wybuchają tylko wtedy, gdy nastąpi silny
zapłon inicjujący.
Otrzymywanie
Nadtlenki wodoru produkuje się głównie metodą antrachinonową (przez cykliczną redukcję wodorem, a
następnie utlenianie powietrzem 2-etyloantrachinonu, z wydzieleniem H2O2). Dawniej otrzymywano w procesie
elektrolizy wodorosiarczanu (VI) amonu i kwasu siarkowego (VI), a także
działając kwasami na nadtlenki.
Zastosowanie
Inne hasła zawierające informacje o "nadtlenek wodoru":
Oddychanie komórkowe
ubichinon i oddaje je na tlen, co prowadzi do wytworzenia H2O2. Powstały
nadtlenek wodoru
rozkładany jest na wodę i tlen przez enzym charakterystyczny dla ...
Aldehyd glicerynowy
glicerynowy otrzymuje się poprzez łagodne utlenianie
gliceryny
. Jako
utleniacz
może być stosowany
nadtlenek wodoru
w obecności soli
żelaza
. Obok aldehydu w tych warunkach powstaje ...
Deoksyryboza
...
Alkohole
...
Ziemia
...
Grupa karbonylowa
...
Katastrofa elektrowni jądrowej w Czarnobylu
...
Czarnobyl
...
Syriusz
...
Łańcuch oddechowy
...
Inne lekcje zawierające informacje o "nadtlenek wodoru":
203 Okres międzywojenny na świecie. Postęp techniczny i kryzys gospodarczy (plansza 3)
...
Wiązania chemiczne w świetle mechaniki kwantowej (plansza 18)
...
Stechiometria wzorów i równań chemicznych (plansza 36)
...
|